Los liposomas fueron descubiertos por primera vez por el Hematólogo británico Alec D. Bangham en 1965. Al estudiar el comportamiento de dispersión de los fosfolípidos en el agua, observó que las moléculas de fosfolípidos formaban espontáneamente estructuras de vesículas multicapa similares a las de las membranas biológicas. En ese momento, la investigación se centró principalmente en la química física básica y la simulación de membrana biológica.
Los investigadores comenzaron a darse cuenta de que los liposomas podían encapsular sustancias solubles en agua y solubles en lípidos, proporcionando un portador potencial para la administración de fármacos. Por ejemplo, en el laboratorio, se encapsularon en liposomas moléculas de modelo de fármaco simple como los colorantes fluorescentes para observar sus características de encapsulación y liberación.
Con una mayor comprensión de la estructura y propiedades de los liposomas, comenzaron a explorarse sus aplicaciones en el campo médico. Este periodo se centró principalmente en la entrega de fármacos antitumorales.
Por ejemplo, algunos fármacos quimioterapéuticos se encapsularon en liposomas como la doxorrubicina, intentando cambiar la farmacocinética y la distribución tisular de los fármacos mediante la encapsulación de liposomas, y reducir la toxicidad de las drogas a los tejidos normales. Sin embargo, los primeros liposomas tenían problemas como poca estabilidad y ser eliminados fácilmente por el sistema mononuclear-fagocito (MPS). Tuvieron un tiempo de circulación corto en el cuerpo y fueron eliminados por el sistema inmunológico antes de que pudieran ejercer plenamente su eficacia, lo que limitó enormemente sus aplicaciones clínicas.
Para superar el problema del corto tiempo de circulación de los liposomas tradicionales en el cuerpo, Los científicos introdujeron la tecnología de liposomas modificados con polietilenglicol (PEG). El PEG es un polímero hidrófilo. Cuando se une a la superficie de los liposomas, puede formar una película hidratada alrededor de los liposomas.
Esta película hidratada puede reducir la interacción entre los liposomas y las proteínas plasmáticas, reduciendo así el reconocimiento y la captación de liposomas por el sistema mononuclear-fagocito. Por ejemplo, Doxil, el primer fármaco liposomal de larga circulación comercializado en el mundo, es un liposoma modificado con PEG que encapsula doxorrubicina. La aparición de Doxil extendió en gran medida el tiempo de circulación de los liposomas en la sangre, lo que permitió que los fármacos tuvieran más oportunidades para llegar a los tejidos tumorales y mejorar el efecto terapéutico de los fármacos.
Los investigadores realizaron estudios en profundidad sobre los liposomas modificados con PEG, incluida la optimización del peso molecular del PEG, el método de conexión y la composición de los liposomas.
Al mismo tiempo, el alcance de la aplicación de los Liposomas de circulación prolongada se expandió de los fármacos antitumorales a otros campos, como la administración de medicamentos antiinflamatorios y antibióticos. Por ejemplo, en el tratamiento de algunas enfermedades inflamatorias crónicas, los Liposomas de circulación prolongada que encapsulan medicamentos antiinflamatorios pueden hacer que los medicamentos se acumulen mejor en los sitios inflamatorios, aumentar la concentración local de medicamentos, y reducir los efectos secundarios sistémicos.
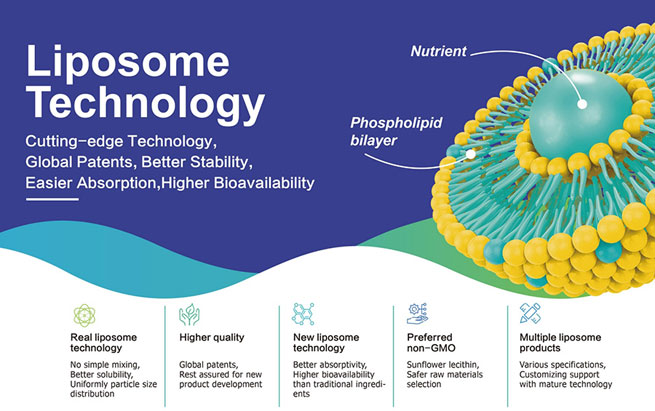
Para mejorar aún más el efecto terapéutico de los liposomas y permitirles administrar medicamentos con mayor precisión a las células enfermas, surgió la tecnología de los liposomas dirigidos. Entre ellos, conjugar anticuerpos contra la superficie de los liposomas es una estrategia importante.
Por ejemplo, al conectar anticuerpos contra antígenos específicos en la superficie de las células tumorales a la superficie de los liposomas, los liposomas pueden reconocer con precisión y unirse a las células tumorales como "misiles". Este liposoma dirigido puede aumentar la absorción de fármacos en las células tumorales y reducir su distribución en los tejidos normales. Se ha aplicado en la investigación del tratamiento de diversos cánceres como el cáncer de mama y el cáncer de pulmón.
Además de los anticuerpos, también se pueden usar otros ligandos para lograr la selección de liposomas. Por ejemplo, se pueden utilizar algunos ligandos de molécula pequeña tales como ácido fólico y transferrina. El receptor de ácido fólico se sobreexpresa en la superficie de muchas células tumorales, mientras que se expresa a un nivel relativamente bajo en la superficie de las células normales.
Por lo tanto, al conectar el ácido fólico a la superficie de los liposomas para administrar fármacos, los liposomas pueden unirse preferentemente a las células tumorales. Este sistema de orientación ligando-liposomas tiene ventajas como un costo relativamente bajo y una preparación fácil, y también se ha aplicado ampliamente en la investigación del tratamiento de tumores y algunas otras enfermedades (como enfermedades cerebrales, usando transferrina para apuntar a los receptores de la barrera hematoencefálica).
Los liposomas inteligentes pueden cambiar su estructura y propiedades de acuerdo con los cambios en el entorno circundante, como el pH, la temperatura y la concentración de enzimas. En el microambiente del tumor, el pH suele ser más bajo que en los tejidos normales. Los liposomas sensibles al pH pueden aprovechar esta característica.
Por ejemplo, un liposoma sensible al pH puede diseñarse para permanecer estable en condiciones de pH fisiológico normales. Cuando llega al microambiente ácido del tumor, la estructura del liposoma cambia, como un aumento en la permeabilidad de la membrana, liberando así rápidamente el fármaco. Este Tipo de liposoma sensible al medio ambiente puede mejorar la eficiencia de liberación del fármaco en el sitio de la lesión y mejorar aún más el efecto terapéutico.
Los liposomas multifuncionales combinan múltiples funciones, como circulación prolongada, focalización y capacidad de respuesta al medio ambiente. Por ejemplo, un liposoma puede tener simultáneamente una modificación de PEG para extender el tiempo de circulación, anticuerpos para las células tumorales Diana y un mecanismo de liberación de fármaco sensible al pH.
El concepto de diseño de este liposoma multifuncional es maximizar la precisión y eficacia de la administración de fármacos. Tiene un gran potencial de aplicación en escenarios de tratamiento de enfermedades complejas, como la terapia tumoral combinada o la terapia con múltiples objetivos.
Los liposomas cocargados de Natural Field pertenecen a la tecnología innovadora de los liposomas inteligentes, utilizando ginsenósidos en lugar de colesterol como un nuevo tipo de portador, que puede lograr una mayor biodisponibilidad.